1.1 Introduction
L’agriculture génère des quantités importantes de sous-produits qui ne sont généralement pas intrinsèquement dangereux, mais la forte teneur en matière organique, et le fait que la production soit concentrée dans une période particulière de l’année pose des problèmes potentiels de pollution. Ainsi l’utilisation efficace des déchets de l’industrie agro-alimentaire est d’une grande importance non seulement pour minimiser l’impact environnemental, mais aussi pour une meilleure rentabilité (Ping et al., 2011).
L’industrie du vin constitue un élément important de l’économie en plusieurs régions du monde, et la vigne est l’une des plus importantes cultures de fruits, avec plus de 60 millions de tonnes produites chaque année (FAO STAT base de données).
Le marc de raisin est constitué de peau, de pulpe, de pépins et de rafles et est obtenu après pressurage du raisin. Il représente environ 20% en masse du raisin récolté (Laufenberg et al., 2003). La production annuelle de marc de raisin en France est actuellement d’environ 700 000 tonnes. Les voies de valorisation actuelles des marcs (alimentation animale et fertilisant) ne sont pas satisfaisantes et posent des problèmes économiques et environnementaux. En effet, les taux élevés de polyphénols (Torres et al., 2002 ; Kammerer et al., 2004) de cette ressource sont un désavantage pour leur utilisation en alimentation animale et entraînent une inhibition de la germination des plantes (Morthup et al., 1998).
Le développement et l’utilisation des matières renouvelables suscitent actuellement un intérêt important. De nombreuses recherches menées sur l’intégration de produits naturels dans les procédés industriels ont vu le jour. Ce fût le cas notamment dans l’industrie du panneau de bois avec un objectif précis de diminuer voire de remplacer intégralement les résines à base de dérivés pétroliers utilisées actuellement (Pizzi, À, 2006).
Malgré des recherches qui se développent de jour en jour autour de cette thématique de «colles vertes», les applications industrielles restent peu développées pour plusieurs raisons: les coûts qui doivent défier la rude concurrence de ceux engendrés par l’utilisation de colles synthétiques, l’aspect technique pour obtenir des performances au moins égale à celles utilisées actuellement (Navarrete Fuentes, 2011), et la disponibilité des matières premières.
1.2 Objectifs de l’étude
Suite à une étude préliminaire réalisée à l’échelle laboratoire au LERMAB, il a été mis au point une méthode d’extraction des tanins en vue d’une application « adhésif vert » pour l’industrie du bois, et plus particulièrement des panneaux de particules. L’utilisation d’adhésifs verts, notamment à base de tanins condensés, a déjà été mise au point pour certaines écorces d’arbres comme le mimosa ou le quebracho (Gambier, 2011).
Bien que de nombreuses méthodes d’extraction des tanins de matière végétale puissent être employées au laboratoire, les techniques industrielles sont des procédures simples, utilisant de l’eau en tant que solvant, à température comprise entre 70 °C et 100 °C, généralement en présence d’une base (carbonate, bicarbonate) et de sulfite de sodium ou métabisulfite (Pizzi, 2003).
Le but de notre projet est double :
– Optimiser les conditions d’extraction dans l’optique d’un développement industrie.
– Définir une méthode de suivi chromatographique du procédé d’extraction permettant de mieux caractériser les extraits.
Dans ce travail, nous nous proposons d’agir sur trois (3) facteurs :
-1° faire varier les proportions de base afin de déterminer les quantités optimales;
-2° remplacer Na2CO3 par NaOH, une base plus facilement accessible au niveau industriel;
-3° étudier l’effet de l’ajout d’urée dans le milieu réactionnel.
Les extraits seront ensuite analysés par des techniques utilisées au laboratoire (Temps de gel, RMN…). Nous nous intéresserons également au développement d’une méthode d’analyse par Chromatographie d’Exclusion Stérique.
1.3 Organismes
1.3.1 UNGDA
L’Union Nationale des Groupements de Distillateurs d’Alcool a été créée le 10 juillet 1946 par les professionnels impliqués dans la production d’éthanol agricole par distillation. Aujourd’hui, l’UNGDA représente l’ensemble des producteurs français d’éthanol utilisant comme matières premières la betterave, les céréales, des produits viniques ou encore de la canne à sucre pour les territoires d’outre mer.
L’UNGDA, centre technique de la profession, est impliquée dans les programmes de R&D stratégiques pour la filière sous le contrôle d’un Conseil Scientifique et d’un Comité de Pilotage. Une activité de contrôle des produits sortant des distilleries ou contenant de l’éthanol est également réalisée en routine par le laboratoire.
Enfin, des missions de services (études, conseils, formation, Kamoran…) sont réalisées auprès de la profession mais également avec ses clients et ce dans le monde entier.
L’UNGDA est également l’interface de la profession auprès des instances administratives françaises ou européennes pour tous les problèmes d’ordre technique, sécuritaire, réglementaire ou normatif liés à l’éthanol.
1.3.2 LERMAB
Créé en 1993, le LERMAB EA4370 est un laboratoire pluridisciplinaire localisé en partie à la Faculté des Sciences et Techniques à Vandoeuvres en partie à L’Ecole Nationale Supérieure des Technologies et Industries du Bois (ENSTIB) à Epinal. Misant sur une approche cognitive basée sur des compétences scientifiques dans des domaines très variés tels que la biologie, la chimie, la physicochimie, la physique, le génie des procédés, la mécanique ou le génie civil, le laboratoire développe des recherches fondamentales et appliquées en relation avec le bois et les fibres naturelles impliquant de considérer le matériau de l’échelle macroscopique jusqu’au niveau moléculaire. De par son positionnement particulier lié à la nature de son objet d’étude, le laboratoire joue un rôle privilégié d’interface entre la recherche et les industries de la filière bois au travers de collaborations avec différents centres de transfert technologique.
D’une manière générale, les recherches menées au laboratoire ont pour but de développer l’utilisation de la ressource lignocellulosique en tant que matériau d’une part, et en tant que source de matières premières pour des applications dans les domaines de la chimie et de l’énergie au travers du développement d’écoproduits ou procédés s’inscrivant dans une démarche de développement durable, d’autre part.
Le laboratoire compte un peu plus d’une quarantaine de permanents dont une trentaine d’enseignants-chercheurs et une trentaine d’étudiants en moyenne, selon les années inscrits en Master ou Doctorat. Il joue un rôle important tant au niveau de la formation par la recherche, qu’au niveau de la formation initiale en participant activement aux enseignements dans le domaine du bois dispensés à l’ENSTIB ou dans le cadre de la spécialité Bois Fibres Énergie Environnement (BF2E) du master FAGE. L’implication du laboratoire est également importante dans des disciplines plus traditionnelles comme la chimie, la chimie physique ou le génie des procédés au niveau Licence comme au niveau Master.
Ce stage s’est déroulé dans les locaux du groupe « valorisation chimique de la biomasse » de l’axe de recherche Matériau dirigé par le professeur Nicolas Brosse au sein de la Faculté des Sciences et Technologies de Vandoeuvre-lès-Nancy. Les travaux menés par ce groupe de recherche visent à la valorisation des ressources lignocellulosiques à travers la notion de bioraffinerie. Le but est donc de trouver des procédés de fractionnement des composants de la biomasse pour pouvoir la valoriser dans son ensemble. Ces recherches font appel à des notions dans les domaines de l’énergie, des matériaux, de l’agro-alimentaire, de la chimie ou de la biochimie.
1.4 Rappels bibliographiques
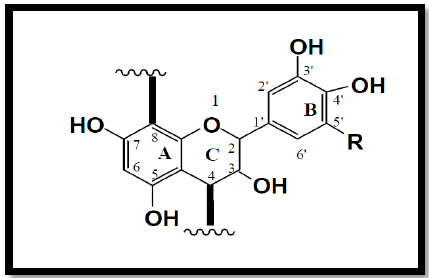
Les tanins de marc de raisin sont principalement composés de proanthocyanidines ou tanins catéchiques. Ce sont des composés formés à partir d’unités monomériques ou polymériques de flavan-3-ols (figure 1) (Haslam, 1980 ; Escribo-Bailon et al., 1992).
Les proanthocyanidines sont composées d’unités procyanidine et prodelphinidine qui sont reliées entre elles par une liaison C4-C8 (Pizzi, 1993, voir figure 1). Ce contenu polyphénolique élevé constitue un inconvénient pour une utilisation des marcs comme aliments pour animaux. Ils pose des problèmes de pollution potentielle lorsque il est utilisé comme engrais pour le sol (Morthup et al., 1998).
R=H : procyanidine ; R=OH : prodelphinidine
Figure 1 : Structure chimique de proanthocyanidines (Pizzi, 1993).
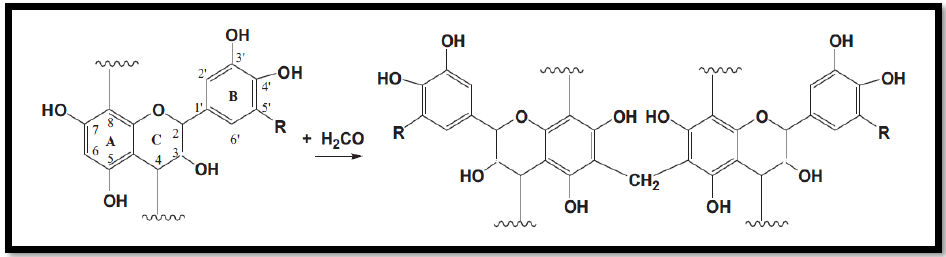
Les colles de bois issues de tanins condensés-formaldéhyde ont été utilisées industriellement depuis les années 1970, pour le collage du bois intérieur et extérieur tels que les panneaux de particules et de contreplaqué (Pizzi, 2003). Elles sont obtenues par durcissement des polymères flavonoïdes par polycondensation avec le formaldéhyde impliquant leurs cycles réactifs comme le montre la figure 2.
Ainsi, il a été démontré que les tanins condensés sont à la fois chimiquement et économiquement intéressants pour la préparation d’adhésifs. Ils peuvent être correctement utilisés en tant que substituts pour le phénol dans la production de résines. Les tanins condensés utilisés dans les études précédentes sont généralement extraits de l’écorce de divers arbres comme le mimosa, le quebracho ou le pin (Panamgama, 2007).
Les techniques industrielles d’extraction sont des procédés simples, utilisant de l’eau comme solvant, à une température comprise entre 70 °C et 100 °C, généralement en présence d’une base (carbonate, bicarbonate) et de sulfite de sodium ou métabisulfite (Tondi and Pizzi., 2009; Lei et al., 2008; Pichelin et al., 2006, Pizzi, 2003).
R=H : procyanidine ; R=OH : prodelphinidine
Figure 2 : Structure chimique de proanthocyanidines et sa réaction avec le formaldéhyde.(Ping et al., 2011).
A chaud, et en présence d’acides minéraux forts, les tanins sont susceptibles de réagir de deux manières différentes :
– Une réaction de dégradation des polymères qui mène à la formation de catéchine et d’anthocyanidines (Navarrete Fuentes, 2011).
– Une condensation résultant de l’hydrolyse des hétérocycles (liaisons p-hydroxybenzyléther). Les ions p-hydroxybenzylcarbonium créés se condensent alors avec les sites nucléophiles d’autres unités de tanin pour former les phlobaphenes (Navarrete Fuentes, 2011).
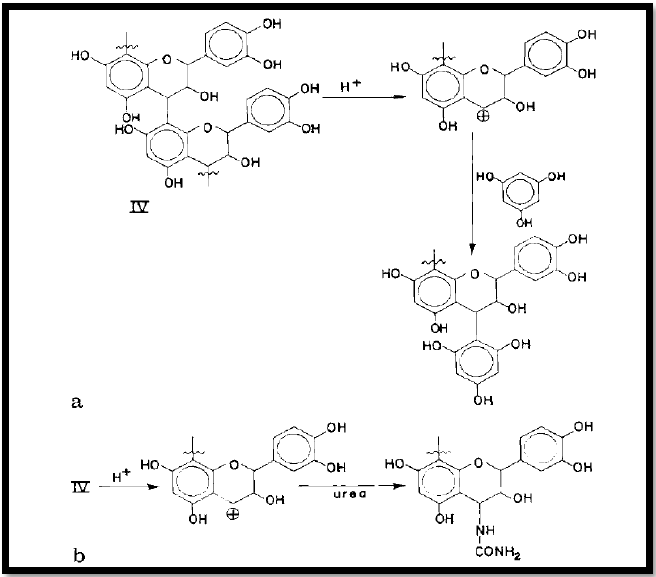
Le rendement du tanin de pin extrait pour une utilisation comme adhésif pour le bois peut être considérablement augmenté en réduisant au minimum l’autocondensation des tanins en phlobaphenes ce par l’addition de petites quantités d’un nucléophile (figure 3) l’urée (Sealy-Fisher et Pizzi., 1992).
Figure 3 :
a – Mécanisme de clivage de la liaison du tanin de pin inter-flavonoïde dans l’acide et du blocage de la réaction de l’autocondensation du tanin de phloroglucinol ou de résorcinol.
b – Mécanisme suggéré de l’action de l’urée dans le blocage dans la forme de carbocation par le clivage de liaisons inter-flavonoïde et de son blocage de l’autocondensation de tannin. (Sealy-Fisher et Pizzi., 1992).
En autre, la sulfitation des tanins est l’une des réactions les plus anciennes et les plus utiles en chimie des flavonoïdes et peut être particulièrement utile dans la préparation des adhésifs à base de tanin. La sulfitation offre généralement une viscosité des tanins plus faible et augmente la solubilité (Pizzi, 1989).
Les deux effets sont dus aux quatre (4) facteurs ci-dessous décrits.
– L’élimination du groupe éther étherocyclic, qui est hydrofuge. En effet, les solutions de tanins extraits dans l’eau ne sont pas de vraies solutions, mais des suspensions hydrocolloïdes.
– L’introduction d’un groupe sulfonique et un autre groupe hydroxyle, tous deux hydrophiles.
– La diminution de rigidité de polymère, et une liaison hydrogène intermoléculaire obtenue par l’ouverture de l’hétérocycle.
– Hydrolyse acide des gommes hydrocolloïdes et de la liaison entre des motifs flavonoïdes.
Les études antérieures effectuées au LERMAB à partir de marcs de raisin ont démontré que l’utilisation d’ions sulfites pouvait permettre d’une part d’augmenter les rendements d’extraction et d’autre part, d’améliorer les propriétés adhésives des extraits de tanins. Les conditions réactionnelles retenues étaient de 2.5% Na2CO3, 2.5% Na2SO3.
De nombreuses méthodes chromatographiques ont été décrites dans la littérature pour analyser les proanthocyanidines (Nonier et al., 2004). La méthode d’HPLC phase normale et en phase inverse peut être utilisée pour séparer les proanthocyanidines. Cependant, ces méthodes sont limitées dans leur capacité à fournir toutes les informations concernant les distributions de masses moléculaires.
La Chromatographie d’Exclusion Stérique (SEC) est la méthode couramment employée pour déterminer la masse moléculaire des polymères (Nonier et al., 2004);
Cependant, la présence de groupes hydroxyles dans les molécules de tanin peut favoriser les interactions par adsorption sur le gel de la phase stationnaire ou la formation de liaisons intermoléculaires par liaison hydrogène, ce qui conduirait à l’estimation incorrecte de la masse moléculaire (Nonier et al., 2004).
Ces phénomènes peuvent être minimisés par l’utilisation de phases mobiles très polaires, telles que le diméthylsulfoxyde (DMSO), diméthylformamide (DMF), ou le tétrahydrofuranne (THF). Une autre procédure consiste à protéger les groupes hydroxyles en tant que dérivés acétylés, dérivés méthylés ou dérivés silylés. L’utilisation simultanée d’un éluant tel que le THF et de tanins acétylés donne de meilleurs résultats pour l’étude des distributions de masses moléculaires des tanins et d’autres biopolymères (Cadahia et al., 1996).
Dans le cadre du présent travail, des expériences ont été menées, afin d’analyser l’influence des concentrations des réactifs et des variations de pH ainsi que l’ajout de l’urée sur le taux d’extraction des tanins.
Les extraits obtenus ont notamment été analysés par Chromatographie d’Exclusion Stérique.
Page suivante : 2 Matériels et méthodes
Retour au menu : Extraction et Analyse de polyphénols de marcs de raisin