Avant de commencer la fabrication de notre boisson « Arbojus», des analyses physico-chimiques et microbiologiques sont effectuées sur les ingrédients Miel «Al-Shifa», Jus de citron, Eau « Texanna ».
II.8.1. Contrôle de qualité des ingrédients
a. Analyses physico-chimiques
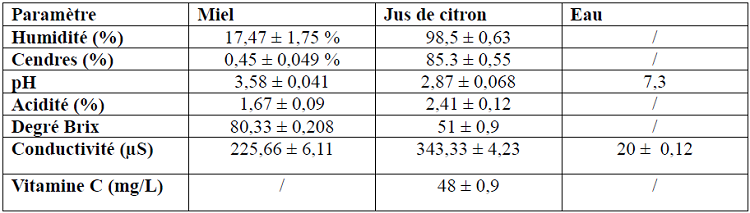
Le tableau 15 représente les paramètres physico-chimiques des ingrédients (miel, jus de citron et eau).
Tableau 15 : Résultats des analyses physico-chimiques des ingrédients
b. Analyses microbiologiques
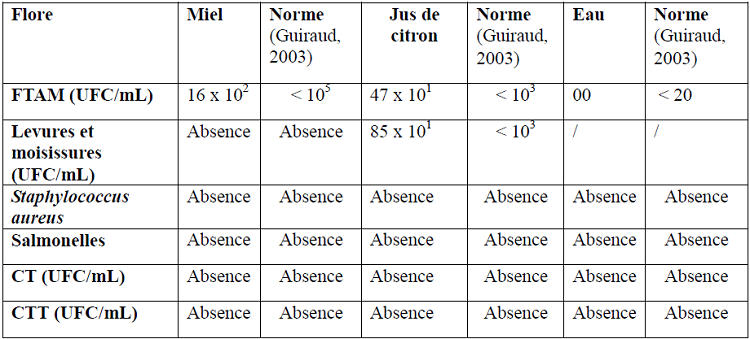
Les résultats de contrôle microbiologique de ces ingrédients sont résumés dans le tableau suivant.
Tableau 16 : Résultats des analyses microbiologiques des ingrédients
Selon les résultats de contrôle physico-chimique et microbiologique des ingrédients utilisés dans la fabrication de notre boisson, on constate qu’ils sont conformes aux normes, et de bonne qualité.
II.8.2.Test de toxicité du gel
L’administration du gel ne provoque aucun changement concernant le comportement et l’état des rats durant les 1ères quatre heures après son administration par gavage.
Ces résultats nous permettent de commencer la fabrication de notre boisson à partir du gel d’Aloe arborescens.
II.8.3. La boisson « Arbojus»
La boisson « Arbojus» (photo 06) est fabriquée selon le diagramme de fabrication (3) déjà cité dans la partie expérimentale.
Photos 06 : La boisson fabriquée « Arbojus» avec l’emballage et l’étiquetage proposé
II.8.4. Contrôle de qualité du produit fini
II.8.4.1. Paramètres physico-chimiques
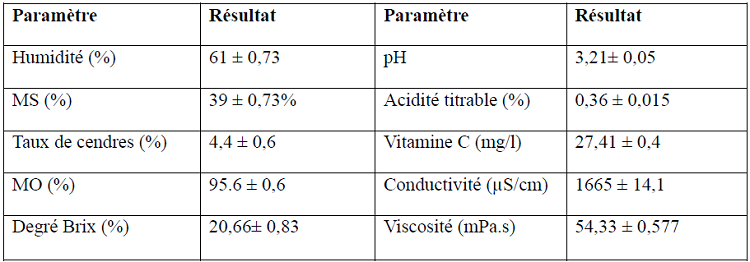
Le tableau suivant résume les résultats obtenus des paramètres physico-chimiques de notre boisson.
Tableau 17 : Paramètres physicochimiques de la boisson fabriquée
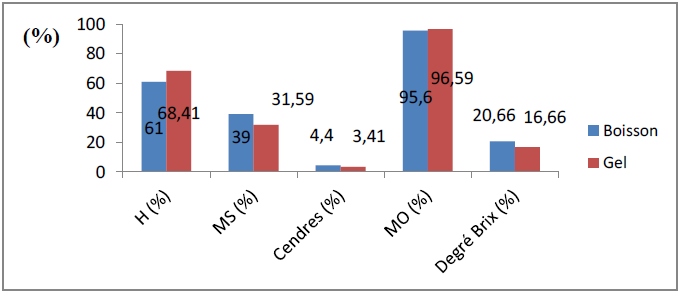
La figure 22 représente la différence entre les teneurs en humidité, cendres et degré Brix du gel et de la boisson fabriquée.
Figure 22 : Comparaison des teneurs en humidité, matière sèche, cendres et matière organique et degré Brix entre le gel et la boisson fabriquée
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
– Humidité et matière sèche
Selon la figure ci-dessus notre boisson a un taux d’humidité égal à 61 ± 0,73%, la matière sèche constitue 39 ± 0,73%.
En comparant ces résultats à ceux obtenu avec le gel qui a une humidité de 68,41 ± 0,38% et le miel a (17,47 ± 1,75%), on trouve que le taux d’humidité de notre boisson est inférieur à celui du gel, on peut constater l’effet du miel sur l’abaissement de l’humidité de notre produit, sans éliminer l’effet de la pasteurisation pendant 15 minutes.
– Teneur en cendres
D’après la figure 22, les cendres constituent 4,4% ± 0,6% du poids total de la boisson, et la matière organique constitue 95,6% ± 0,6%.
On peut remarquer que le taux en cendres de la boisson est supérieur à celui du gel qui est l’ingrédient principal de notre boisson, le gel a eu un taux en cendres égal à 3,41% ± 0,79%, cette augmentation est principalement due à l’intervention du miel qui a un taux en cendres très bas et égal à 0,45 ± 0,049%, mais elle reste acceptée et on peut dire que la teneur en matière minérale n’est pas influencée.
– Le degré Brix
En lisant le tableau précédent, la boisson a un degré Brix égal à 20,66± 0,83%, cette valeur représente la teneur en matière solide soluble dans notre boisson, elle est supérieure à celle du gel (16,6 ± 1,6), en revanche les valeurs obtenues pour le miel (80,33 ± 0,208%) et le jus de citron (51 ± 0,9%) sont supérieures à celle-ci.
La figure 23 illustre la différence du pH et acidité titrable entre le gel et la boisson.
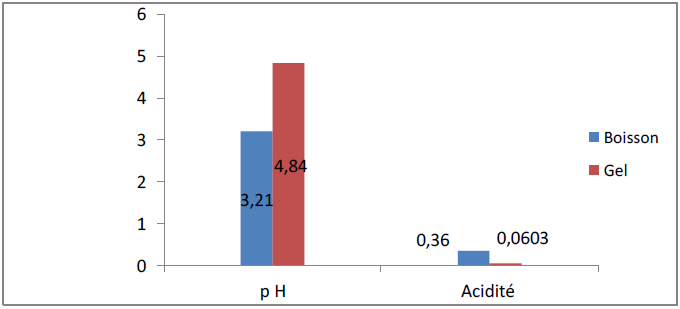
Figure 23 : Comparaison entre pH et acidité du gel et de la boisson
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
– pH et acidité
La figure 23 montre que le pH de notre boisson est de 3,21± 0,05, cette valeur est inférieure à celle du gel (4,84 ± 0,05) et du miel (3,58 ± 0,041), mais elle reste supérieure à celle du jus de citron (2,87 ± 0,068).
On peut remarquer l’effet du miel mais beaucoup plus du jus de citron sur l’abaissement du pH sans éliminer l’effet de l’acide citrique ajouté, cette diminution est bénéfique et considérée comme un avantage pour notre boisson, en raison du rôle important de pH dans la conservation des denrées alimentaires, en fait, un pH acide aide à éliminer une grande partie de la flore microbienne.
Concernant l’acidité, la figure précédente montre que l’acidité de notre boisson est 0,36 ± 0,015, cette valeur est supérieure à celle du gel (0,0603% ± 0,003 %.), mais elle est inférieure à celles du miel (1,67% ±0,092%) et de jus de citron (2,41% ± 0,12%).
On peut constater l’effet du jus de citron et du miel avec l’acide citrique additionné sur l’augmentation de l’acidité de la boisson, cette augmentation est accompagnée par un abaissement de pH, ce qui rend notre boisson résistant aux agents de détérioration microbiologique.
La figure 24 illustre la différence de la conductivité électrique, la turbidité et la viscosité entre le gel et la boisson.
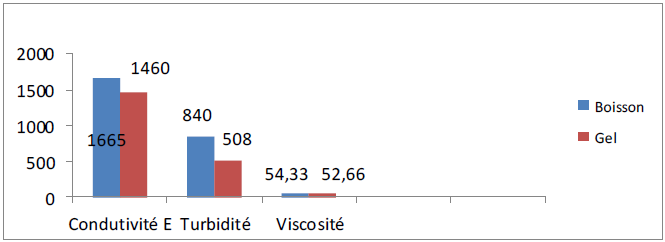
Figure 24 : Comparaison entre conductivité électrique, turbidité et viscosité du gel et de la boisson fabriquée
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
– La conductivité électrique
Selon la figure 24, la conductivité électrique de la boisson était 1665 ± 14,1 μS/cm, cette valeur est supérieure à celles du gel ayant une conductivité électrique égal à 1460 ± 6,24 μS/cm, de jus de citron (343,33 ± 4,23 μS/cm) et du miel (225,66 ± 6,11%).
On remarque une petite augmentation de la conductivité électrique dans notre boisson, cela peut être justifié par l’augmentation des ions minéraux qui sont responsables de la conductivité électrique.
– La turbidité
La figure 24 montre que la turbidité de notre boisson est égale à 840 ± 1,38 UTN, cette valeur est supérieure à celle du gel (508 ± 1,24 UTN), on remarque une augmentation de la turbidité dans la boisson, cette dernière est due aux ingrédients additionnés.
– La viscosité
Selon la figure précédente, la viscosité de notre produit est égale à 54,33 ± 0,57 mPa.s, cette dernière est proche à celle du gel (52,66 ± 0,57 mPa.s), ce qui rend notre boisson visqueuse. La consistance visqueuse de la boisson est le résultat de deux ingrédients visqueux qui sont le miel et le gel.
II.8.4.2. La teneur en éléments minéraux
Les résultats obtenus concernant les concentrations des éléments minéraux de la boisson sont mesurés à partir des courbes d’étalonnage (annexe 2) de chaque élément dosé.
o Les oligoéléments
La figure suivante montre la teneur en oligoéléments dosés dans la boisson.
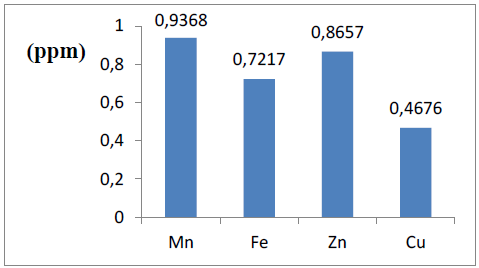
Figure 25 : Teneur en oligoéléments (ppm) de la boisson
Selon l’analyse statistique (Student), les résultats sont significativement différents (p< 0,05).
– Le manganèse
Selon la figure ci-dessus la concentration du manganèse dans notre boisson est 0,9368 ppm, en comparant aux autres oligoéléments dosés, le manganèse est l’élément majeur parmi ceux-ci suivi du zinc.
On peut remarquer aussi que la concentration du manganèse dans la boisson est supérieure à celle trouvée dans l’ingrédient principal qui est le gel, où la concentration était 0,5873 ppm. Cette augmentation est due principalement aux autres ingrédients, le miel et le citron beaucoup plus.
L’augmentation de la concentration en manganèse est un avantage pour notre boisson. En fait, selon Bassetti et Sala (2005), le manganèse est un élément ayant un effet antioxydant puissant, capable de ralentir le processus de vieillissement. En outre les cellules riches en cet élément ont une plus grande capacité de combattre au loin les effets négatifs du large rayonnement de spectre auquel nous sommes exposés quotidiennement.
– Le fer
D’après la figure 25, la concentration du fer dans la boisson est égale à 0,7217 ppm, cette dernière est inférieure à celle du manganèse et du zinc, mais elle est inférieure à celle du cuivre.
On remarque aussi que la concentration du fer dans notre boisson est supérieure à celle du gel qui a une concentration de 0,6199 ppm, cette augmentation est due principalement aux ingrédients additionnés, elle reste bénéfique pour notre boisson.
En fait, le fer est un constituant essentiel d’hémoglobine, l’élément responsable du transport de l’oxygène lui donnant sa couleur rouge lorsqu’il est oxygéné, sa carence cause une pathologie appelée l’anémie (Bassetti et Sala, 2005).
– Le Zinc
Selon la figure précédente la concentration du zinc dans notre boisson est 0,8657 ppm, il est classé deuxième après le manganèse en comparant sa concentration aux autres oligoéléments dosés.
La concentration du zinc dans notre boisson est supérieure à celle du gel (0,3076 ppm), on remarque une augmentation de la concentration dans la boisson, celle-ci est due aux ingrédients additionnés, cette augmentation améliore la qualité nutritionnelle et curative de notre boisson.
Le zinc est un oligoélément qui peut stimuler et renforce le système immunitaire, il a un rôle important dans le traitement du diabète. Il règle le métabolisme de sucre de sang dans le foie.
– Le cuivre
Selon la figure précédente, la concentration du cuivre dans notre boisson est égale à 0,4676 ppm, le cuivre présente la concentration la plus basse de tous les oligoéléments dosés de la boisson.
On peut remarquer que la concentration du cuivre dans la boisson est supérieure à celle du gel (0,0911ppm), l’augmentation de la concentration du cuivre dans la boisson est due au miel et au jus de citron, cette augmentation est considérée bénéfique pour notre boisson en raison de l’importance du cuivre dans la santé, il a des propriété anticancéreuse, il agit en tant qu’antioxydant fort, limitant les dommages provoqués par les radicaux libres (Bassetti et Sala, 2005).
o Les métaux lourds
La figure 26 représente les teneurs en métaux lourds dans notre boisson.
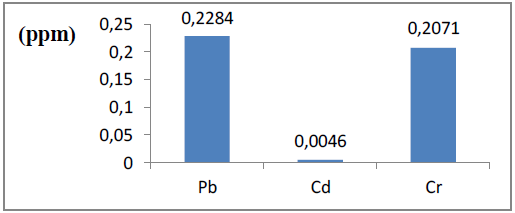
Figure 26 : Teneur en métaux lourds dans la boisson fabriquée
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
– Le plomb
Selon la figure ci-dessus, la concentration du plomb dans la boisson est égale à 0,2284 ppm, c’est la concentration la plus élevée des trois métaux lourds dosés dans la boisson.
Cette concentration est inférieure à la limite permise par le Règlement (CE) № 629/2008 de la Commission Européenne du 2 juillet 2008, où il fixe une limite de 3,0 ppm.
– Le cadmium
La concentration du cadmium dans notre boisson est égale à 0,0046 ppm, c’est la concentration la plus basse de tous les métaux lourds dosés dans la boisson.
La concentration du cadmium dans notre boisson est inférieure la limite décrite dans le règlement (CE) № 629/2008 de la Commission Européenne du 2 juillet 2008, cette dernière est égale à 1 ppm.
– Le chrome
La lecture de la figure ci-dessus permet de constater que la concentration du chrome dans la boisson est proche à celle du plomb (0,2284 ppm), elle est égale à 0,2071 ppm.
II.8.4.3. Teneur en lipides et en sucres totaux
La figure 27 montre la différence de la teneur en sucres totaux et en lipides entre le gel et la boisson.
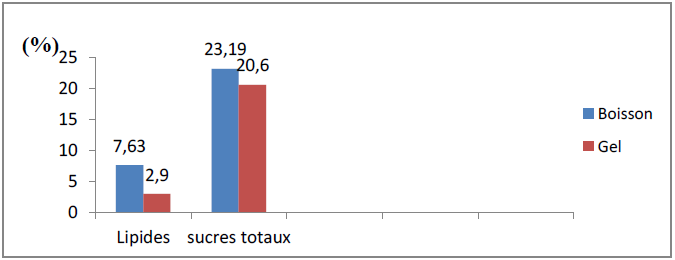
Figure 27 : Comparaison entre les teneurs en sucres totaux et en lipides entre le gel et la boisson
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
Selon la figure 27, les lipides constituent 7,63% du PF de la boisson, on peut constater une augmentation de la teneur en lipides par rapport à celle du gel où les lipides constituent 2,9% du PF.
Cette augmentation est due aux deux ingrédients additionnés, qui sont le miel et le jus de citron. En fait les lipides participent à l’augmentation de la valeur nutritionnelle et par conséquent rendent notre boisson énergétique.
D’après la figure 27, les sucres totaux constituent 23,19 ± 0,73% du PF de la boisson, on peut constater que les sucres sont la partie majeure de notre boisson, en comparant cette valeur à celle du gel où les sucres totaux constituent 20,6 ± 0,9 % du PF, en peut remarquer que le taux de sucres dans notre boisson augmente de 2,59 % par rapport à celui du gel.
Cette augmentation est principalement due au miel qui contient beaucoup de sucres, en donnant à notre boisson une saveur sucrée.
L’augmentation du taux de sucres dans la boisson est considérée un avantage pour notre boisson, en raison de l’augmentation de la valeur énergétique, ce qui rend notre boisson énergétique.
II.8.4.4.Teneur en vitamine C
La figure 28 illustre la différence entre la concentration de la vitamine C dans le gel et la boisson
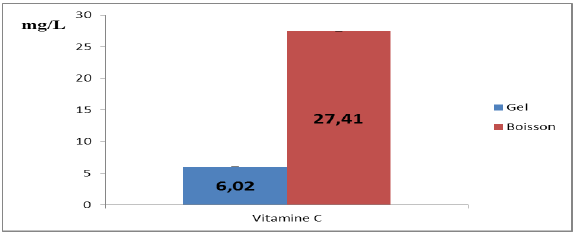
Figure 28 : Comparaison entre la teneur en vitamine C du gel et de la boisson
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
D’après la figure ci-dessus, la concentration de la vitamine C dans notre boisson est égale à 27,41 ± 0,4 mg/L. On peut constater que cette valeur est supérieure à celle du gel (6,02 ± 0,54 mg/L) avec une augmentation de 21,21 mg/L par rapport à la concentration du gel (6,02 ± 0,54 mg/L).
L’augmentation de la teneur en vitamine C est due au jus de citron riche en en cette dernière (48 ± 0 ,9 mg/L), ce qui rend notre boisson d’une valeur nutritionnelle très appréciée.
II.8.5. Composition phyto-chimique
Le tableau suivant récapitule les résultats obtenus concernant les substances secondaires dosés.
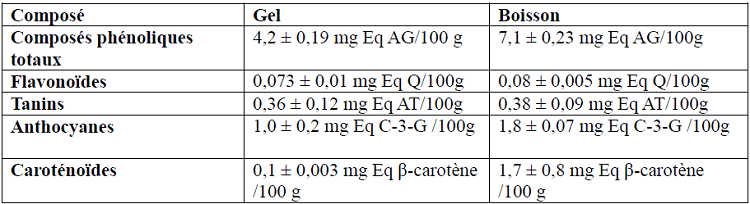
Tableau 18 : Composition phyto-chimique du gel et de la boisson
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
– Teneur en composés phénoliques totaux
Le tableau 18 montre que la concentration des composés phénoliques totaux est égale à 7,1 ± 0,23 mg Eq AG/100g du PF du PF, cette valeur est supérieure à celle du gel (4,2 ± 0,19 mg Eq AG/100 g du PF).
On constate une augmentation de 2,9 mg Eq AG, cette dernière est due principalement au jus de citron, mais aussi au miel.
– Teneur en flavonoïdes
D’après le tableau18, la boisson contient une concentration en flavonoïdes égale à 0,08 ± 0,005 mg Eq Q/100g du PF.
On peut remarquer la différence entre la concentration des flavonoïdes dans notre boisson et celle du gel (0 ,073 ± 0,01 mg Eq Q/100g du PF), il y a une légère augmentation de la concentration des flavonoïdes dans la boisson par rapport à celle du gel.
L’origine de cette augmentation est due principalement au jus de citron qui est riche en ces pigments qui lui donnent la couleur jaune.
Selon Shohaib et al., (2011), les flavonoïdes entrent dans le traitement de plusieurs maladies telles que la pneumonie, le cancer, et les dysenteries amibiennes, ils ont la capacité vasodilatatrice, qui les rend très efficaces dans le traitement des maladies cardiaques.
– Teneur en tanins
Le tableau 18 montre que la concentration des tanins dans notre boisson est égale à 0,38 ± 0,09 mg Eq AT/100g du PF, on peut constater une légère augmentation de la concentration des tanins dans notre boisson par rapport au gel où la concentration des tanins est égal à 0,36 ± 0,12 mg Eq AT/100g du PF.
Cette augmentation est principalement due au jus de citron, mais probablement au miel.
– Teneur en anthocyanes
Selon le tableau 18 la concentration des anthocyanes dans la boisson est égale à 1,8 ± 0,07 mg Eq C-3-G /100g du PF.
On peut remarquer une légère augmentation de la concentration des anthocyanes dans notre boisson par rapport à celle du gel (1,0 ± 0,2 mg Eq C-3-G /100g du PF).
Le jus de citron est le responsable de cette différence en raison de sa richesse en anthocyanes.
– Teneur en caroténoïdes
La concentration des caroténoïdes dans notre boisson est égale selon le tableau 18 à 1,7 ± 0,8 mg Eq β-carotène /100 g du PF.
Le jus de citron est le responsable de l’augmentation de la concentration en caroténoïdes dans notre boisson par rapport à la concentration trouvée dans le gel (0,1 ± 0,003 mg Eq β-carotène /100 g du PF).
Les caroténoïdes augmentent l’activité antioxydante de notre boisson et par conséquent sa capacité curative.
II.8.6. Contrôle microbiologique
Les résultats obtenus concernant la microbiologie de notre boisson sont illustrés par le tableau ci-dessous.
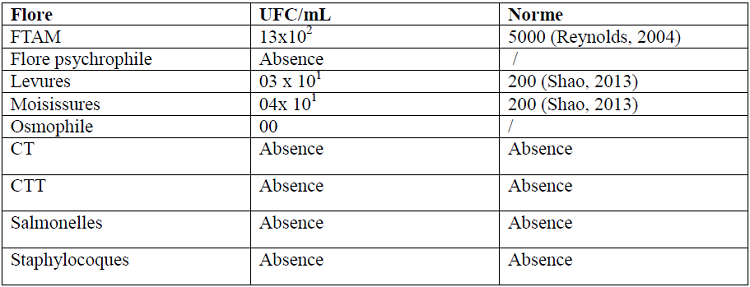
Tableau 19 : Qualité microbiologique de la boisson fabriquée
Selon le tableau ci-dessus, les germes présents dans notre boisson sont : la flore aérobie mésophile (13 x 102 UFC/mL), les levures (30 UFC/mL), et les moisissures (40 UFC/mL).
La flore psychrophile, la flore osmophile, les CT, les CTT, les salmonelles et les staphylocoques sont totalement absents dans la boisson.
En comparant ces résultats aux normes, on peut dire que notre boisson est conforme aux normes et par conséquent de bonne qualité hygiénique.
II.8.7. Analyse sensorielle
Les résultats de l’analyse sensorielle de la boisson «Arbojus» sont résumés dans la figure 29.
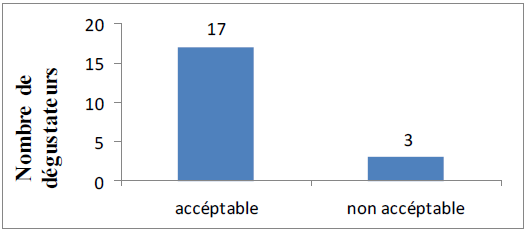
Figure 29 : Résultats de l’analyse sensorielle de la boisson fabriquée
Selon l’analyse statistique (Student), les résultats sont significativement différents (P < 0,05).
Cette étude vise à déterminer le degré d’acceptation de notre boisson. Les résultats obtenus montrent une déférence entre le degré d’acceptation avec 85% des dégustateurs ont accepté la boisson «Arbojus», alors que 15% ne l’acceptent pas.
Cette déférence peut être expliquée par le fait que les dégustateurs recrutés ont des degrés de sensation différents, ou bien ces derniers ont des préférences spécifiques vis-à-vis des boissons.
Ces résultats nos permet de dire que notre boisson «Arbojus» est comestible en point de vue préférences du consommateur.
II.8.8. Essais de stabilité de la boisson fabriquée
Dans le but d’évaluer la stabilité des différentes caractéristiques de la boisson médicinale fabriquée, elle est conservée à différentes températures (température ambiante et à 4°C) avec ou sans pasteurisation pendant 8 jours (selon le diagramme de fabrication déjà cité dans le chapitre précédent) .On obtient alors 4 boissons avec la boisson fraiche avant stockage :
– Boisson pasteurisée conservée à 4°C /8 jours (BPR); (diagramme 03)
– Boisson pasteurisée conservée à température ambiante /8 jours (BPTA); (diagramme 04)
– Boisson non pasteurisée conservée à 4°C /8 jours (BNPR); (diagramme 2)
– Boisson non pasteurisée conservée à température ambiante / 8jours (BNPTA). (diagramme 1)
– Boisson fraiche avant stockage (BFAS).
a. Caractéristiques sensorielles
Les caractéristiques sensorielles de ces boissons après 8 jours de conservation sont : un gout sucré acide, une odeur citronnée – miel, une consistance aqueuse et une couleur jaune foncé, mais on a constaté quelques modifications avec la boisson non pasteurisée conservée à température ambiante, qui avait une odeur du miel dominante. On peut dire que les trois boissons BPR, BPTA et BNPR ont les caractères sensoriels de la boisson BFAS.
b. Analyses physico-chimiques
1. pH et acidité titrable
Les résultats de la mesure du pH et acidité titrable des différentes boissons sont illustrés par la figure suivante.
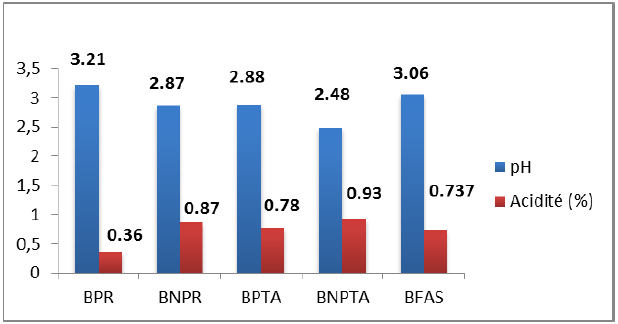
Figure 30 : pH et acidité titrable des quatre boissons fabriquées après 8 jours de stockage avec la boisson fraiche
L’analyse statistique de l’ANOVA révèle que, l’évolution du pH des boissons fabriquées est non significative (P < 0,05) et que l’évolution de l’acidité titrable des boissons (BPR, BPTA, BNPR) présente des différences non significatives entre elles, et significatives comparé à la boisson BFAS.
La lecture de la figure ci-dessus a permet de constater que la valeur la plus basse du pH (2,48 ± 0,09) est marquée dans la boisson BNPTA, avec une valeur d’acidité maximale égale à 0,93 ± 0,013%, alors que BPR a prend la valeur maximale du pH (3,21 ± 0,05) et la valeur minimale de l’acidité (0,36 ± 0,015 %). Les deux autres boissons (BPTA et BNPR) ont eu les valeurs de pH: 2,88 ± 0 ,09 et 2,87 ± 0,012 successivement, avec des valeurs d’acidité titrable égales à 0,78 ± 0,01% et 0,87 ± 0,019% ce qui les considère très acides.
En comparant ses résultats à ceux obtenus avec la boisson BFAS qui a un pH égal à 3,06 ± 0,09 avec une acidité de 0,737 ± 0,018%, on peut constater une légère augmentation de pH de la boisson BPR (3,21 ± 0,05) accompagnée d’une diminution de l’acidité titrable (0,36 ± 0,015 %),cela peut être exprimé par l’effet de la pasteurisation sur les acides contenus dans la boisson BPR. En fait la pasteurisation a détruit une partie des acides dans la boisson BPR ce qui augmente le pH et diminue l’acidité titrable.
Pour les autres boissons ; BNPTA, BPTA et BNPR, on peut remarquer un abaissement de pH accompagné d’une augmentation de l’acidité surtout pour la boisson BNPTA, cette dernière est considérée très acide.
Comme résumé, la boisson idéale c’est BPR qui prend des valeurs de l’acidité et du pH très acceptables. Les autres boissons sont considérées comme acides mais de qualité acceptable à l’exception de la BNPTA.
2. Humidité et matière sèche
Les résultats des valeurs d’humidité et de la matière sèche des boissons fabriquées sont illustrés par la figure ci-dessous :
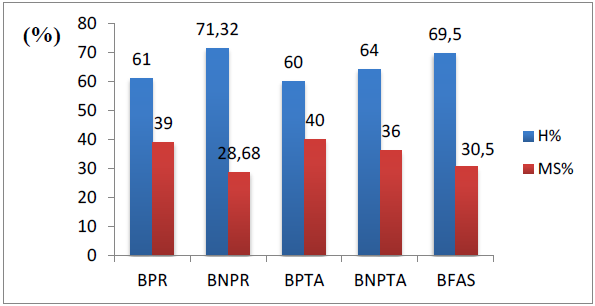
Figure 31 : Humidité et matière sèche des quatre boissons avec la boisson fraiche avant stockage
L’analyse statistique de l’ANOVA révèle que, l’évolution de l’humidité et de la matière sèche des boissons fabriquées sont non significatives (P < 0,05).
En lisant la figure ci-dessus, on peut déduire les informations suivantes : l’humidité a prend sa valeur maximale dans la boisson BNPR avec un pourcentage de 71,32 ± 0,52%, alors que sa valeurs minimale (60± 0,23%) a été enregistrée dans la boisson notée BPTA, les valeurs intermédiaires sont marquées dans les boissons BNPTA, BPR et BFAS avec un pourcentage de 64 ± 0,76%, 61 ± 0, 73 % et 69,5± 086% successivement.
On constate une légère augmentation de l’humidité de 1,82% dans la boisson notée BNPR, cela peut être due à la réfrigération qui peut augmenter le taux de l’eau dans le produit.
On peut dire que la diminution de l’humidité dans les boissons BPR et BPTA est due à la chaleur de la pasteurisation, on peut constater aussi la diminution de l’humidité de la boisson BNPTA, cette diminution est due à la chaleur de stockage (température ambiante).
3. Le degré Brix
Les valeurs du degré Brix des boissons fabriquées sont illustrées par la figure suivante.
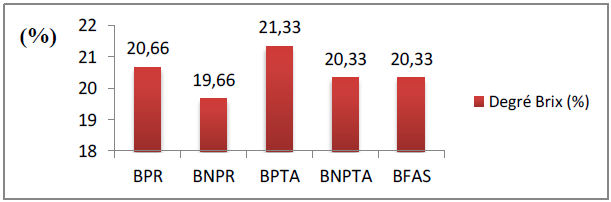
Figure 32 : Le degré Brix des boissons fabriquées
L’analyse statistique de l’ANOVA révèle que, l’évolution de la teneur en solide soluble des boissons fabriquées est non significatives (P < 0,05).
Selon la figure précédente la boisson BPTA a prend la valeur maximale du degré Brix (21,33± 0,16%) et la valeur minimale est marquée par la boisson BNPR (19,66± 0,66%), le degré Brix de la boisson BFAS est égal à celui de la boisson BNPTA.
On peut constater que l’effet de la pasteurisation et du stockage est léger sur la teneur en matière solide soluble.
4. Conductivité électrique
La figure suivante montre les résultats de la conductivité électrique des boissons fabriquées.
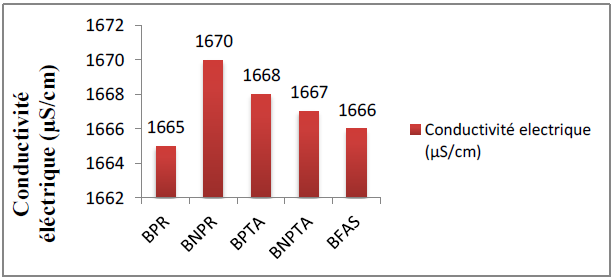
Figure 33 : Conductivité électrique des boissons fabriquées
L’analyse statistique de l’ANOVA révèle que, l’évolution de la conductivité électrique des boissons fabriquées est non significatives (P < 0,05).
La lecture de la figure permet de remarquer l’effet léger de la pasteurisation et du stockage sur la conductivité électriques des boissons, il se trouve une petite différence entre les valeurs obtenues de la conductivité électrique des quatre boissons avec la boisson fraiche avant stockage ne dépassant pas les 5μS/cm.
La valeur maximale est marquée dans la boisson BNPR alors que la valeur minimale est marquée dans la boisson notée BPR.
5. Turbidité
La figure suivante montre les résultats de la turbidité des boissons fabriquées.
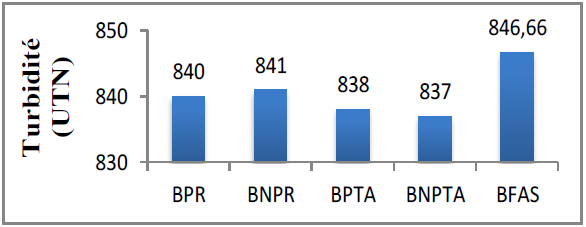
Figure 34 : La turbidité des boissons fabriquées
L’analyse statistique de l’ANOVA révèle que, l’évolution de la turbidité des boissons fabriquées est non significatives (P < 0,05).
D’après la figure ci-dessus, la boisson BFAS a la valeur de la turbidité la plus élevée (846,66 ± 1,52), alors que la valeur minimale est enregistrée par la boisson BPTA (838± 1,22).
On peut dire que la pasteurisation et le stockage ont un effet léger sur notre boisson, les petites différences notées sont de l’ordre d’environ 9 UTN et démontrent que notre boisson est homogène et elle n’est pas influencée par le temps de stockage et la température.
6. Teneur en Vitamine C
La figure 35 montre les teneurs en vitamine C (acide ascorbique) des boissons fabriquées :
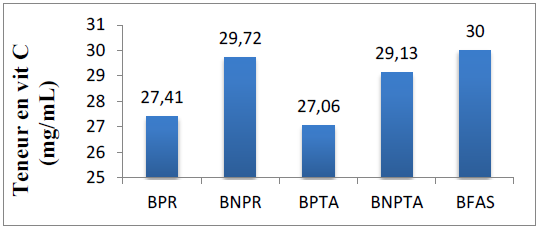
Figure 35 : Teneur en acide ascorbique des boissons fabriquées
L’analyse statistique de l’ANOVA révèle que, l’évolution des teneurs en acide ascorbique des boissons fabriquées est significatives (P < 0,05) et que les boissons pasteurisé ont une teneur en vitamine C inferieur à celles non pasteurisés. Car la chaleur engendre des pertes en vitamine C.
En lisant la figure précédente on peut dire que la teneur en vitamine C a été influencée par la pasteurisation, les boissons pasteurisées BPR et BPTA ont présenté les valeurs minimales de la teneur en vitamine C (27,41 ± 0,4 mg/L et 27,06 ± 0,52 mg/L) alors que les boissons non pasteurisées ont également présenté une légère diminution de la teneur en vitamine C.
II.8.9. Analyses microbiologiques
Les résultats de l’évaluation microbiologique des boissons fabriquées sont illustrés par le tableau suivant :
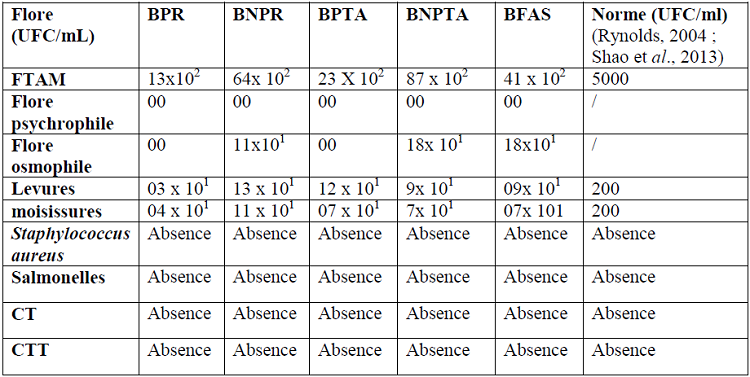
Tableau 20 : Qualité microbiologique des boissons obtenues
Selon les résultats obtenus, on constate l’absence totale des germes suivants : staphylococcus aureus, salmonelles, CT et CTT et la flore psychrophile dans toutes les boissons, avec l’absence de la flore osmophile dans les boissons pasteurisées.
Concernant les autres germes (FTAM, levures et moisissures), les résultats obtenus pour les boissons pasteurisées (pour BPR et BPTA) sont conformes aux normes déjà citées, cependant les boissons non pasteurisées (BNPTA et BNPR) présentent une FTAM qui dépasse la norme, d’où l’intérêt d’appliquer une pasteurisation pour notre boisson afin d’assurer la qualité hygiénique du produit final.
On constate également que les boissons pasteurisées conservées soit à 4ºC ou à température ambiante présentent le même niveau hygiénique, cependant pour les levures et moisissures la boisson réfrigérée possède un taux de germe inférieur à celui de la boisson gardée à température ambiante.
Pour les levures et moisissures et la FTAM, la pasteurisation a diminué le nombre de ces dernières, alors qu’elle élimine toute la flore osmophile. Donc la meilleure façon de conserver notre boisson pasteurisée est de la mettre à 4ºC.
Comme résumé et après les constatations faites sur les paramètres précédents, on trouve que la meilleure façon de conserver et de stocker notre boisson médicinale est de la pasteuriser et la stocker à température de 4°C. Cela ne considère pas que les autres boissons soient de mauvaise qualité, mais pour assurer une bonne salubrité pour notre boisson, il est indispensable de la traiter par la chaleur et stocker au réfrigérateur à 4°C.