a. Teneur en composés phénoliques totaux
La teneur en composés phénoliques totaux est estimée à l’aide de la méthode du Folin-Ciocalteu en utilisant une courbe d’étalonnage à l’acide gallique (annexe 3).
La figure ci-dessous illustre les résultats obtenus concernant la teneur en composés phénoliques totaux dans le gel et les feuille.
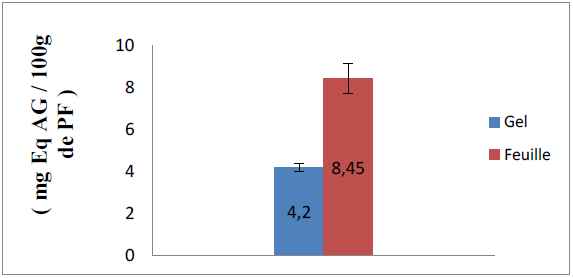
Figure 13 : Teneur en composés phénoliques totaux des extraits du gel et feuilles d’Aloe arborescens
Selon l’analyse statistique, ces résultats sont significativement déférents (P < 0,05).
Selon la figure ci-dessus, la concentration des composés phénoliques totaux dans la feuille est égale à 8 ,45 ± 0,73 mg Eq AG/100 g du PF de la feuille, cette valeur est supérieure à celle du gel où la concentration en composés phénoliques totaux était 4,2 ± 0,19 mg Eq AG/100 du PF.
La valeur trouvée concernant la concentration des composés phénoliques totaux dans le gel est largement inférieure à celles trouvées par Zapata et autres (2013), ce dernier a trouvé que la concentration des composés phénoliques totaux dans le gel d’Aloe arborescens varie entre 12 et 50 mg Eq AG/100g du PF.
Cette différence pourrait être due aux conditions climatiques, au temps de la récolte et aux cultivars, mais aussi à la méthode de dosage elle-même et au solvant d’extraction.
En effet, les conditions d’extraction en terme de température et le nombre d’étapes d’extraction ainsi que l’état et l’origine de l’échantillon en terme de provenance géographique, ne peuvent pas être exclus (Li et al., 2009 ; Suhaj, 2006).
Selon Macheix et ses collaborateurs (2005), la méthode de Folin-Ciocalteu peut présenter des interférences en présence d’autres composés réducteurs que les composés phénoliques comme l’acide ascorbique.
Selon Zapata et ces collaborateurs (2013) la teneur en composés phénoliques totaux est influencée par les saisons de l’année, où ces composés prennent leurs valeurs maximales en été, et minimales en printemps, la température élevée induit l’accumulation des produits phénoliques comme réponse de stresse de la plante.
b. Teneur en flavonoïdes
Les flavonoïdes sont omniprésents chez tous les végétaux. Leur activité est exprimée par leur grande affinité biologique avec les polymères, les métaux lourds et surtout pour leur activité antioxydante. Ce sont les plus actifs parmi les antioxydants végétaux alimentaires. Ils ont en outre une action thérapeutique sur certaines pathologies telles : le traitement des inflammations, des infections virales et du cancer (Morelle, 2006).
La teneur en flavonoïdes est déterminée à partir d’une courbe d’étalonnage à la quercétine (annexe 3), en mg Eq Q/100g du PF. La figure suivante montre les résultats obtenus concernant la teneur en flavonoïdes du gel et de la feuille.
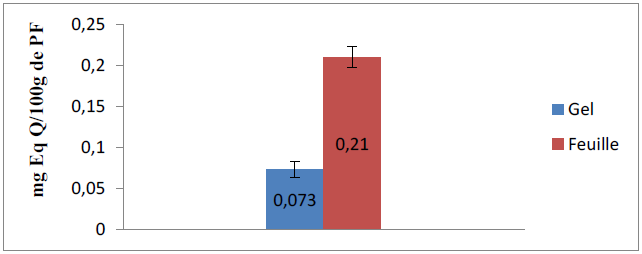
Figure 14 : Teneur en flavonoïdes des extraits du gel et la feuilles d’Aloe arborescens
L’analyse statistique révèle une différence significative entre la teneur en flavonoïdes de la feuille et du gel (P < 0,05).
D’après la figure 14, la concentration en flavonoïdes dans les feuilles est égale à 0,21 ± 0,013 mg Eq Q/100g du PF, alors qu’ils ne constituent que 0,073 ± 0,01 mg Eq Q/100g du PF.
On constate que la concentration des flavonoïdes dans les feuilles est supérieure à celle du gel.
La valeur obtenue concernant la concentration des flavonoïdes dans les feuilles est largement inférieure à celles trouvées par Cardoso et ses collaborateurs (2010), en étudiant les feuilles d’Aloe arborescens, il a trouvé que la concentration des flavonoïdes dans celles-ci varie entre 8 ± 2 mg Eq Q/100g du PF et 14 ± 3 mg Eq Q/100g du PF.
Cette différence est peut être due au temps et aux saisons de la récolte, aux conditions climatiques, et condition d’extraction et du dosage lui-même.
Selon Rawel et ses collaborateurs (2005), les méthodes de conservation et d’exposition à la lumière des plantes peuvent affecter la teneur en flavonoïdes. En effet, ceux-ci sont sensibles à l’oxydation, ce qui pourrait expliquer ces différences.
Cardoso et ses collaborateurs (2010), a trouvé que la concentration des flavonoïdes dans les feuilles d’Aloe arborescens est variable en fonction de saisons et des solvants utilisés, les flavonoïdes prennent leur concentration maximale en automne, alors que la concentration minimale a été marquée en été. Il a constaté aussi que les concentrations des flavonoïdes obtenues à partir des extraits chloroformiques sont supérieures à celles obtenues en utilisant l’éthanol comme solvant d’extraction.
c. Teneur en tanins
Les tanins sont des formes phénoliques capables de se lier aux protéines en solution et de les précipiter (Macheix et al., 2005).
La teneur en tannins des échantillons est déterminée à partir de la courbe d’étalonnage réalisée avec de l’acide tannique (annexe 3).
Les résultats obtenus sont résumés dans la figure suivante.
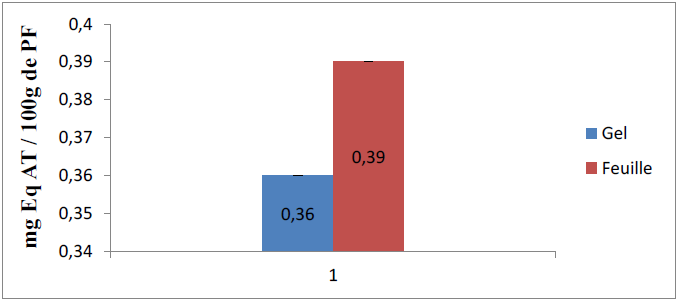
Figure 15 : Teneur en tannins des extraits du gel et de la feuille d’Aloe arborescens
L’analyse statistique révèle une différence significative entre la teneur en tannins de la feuille et du gel (P < 0,05).
La figure ci-dessus montre que la teneur des feuilles en tanins est égale à 0,39 ± 0,1 mg Eq AT/100g du PF, supérieure à celle trouvée dans le gel où la concentration des tanins égale à 0,36 ± 0,12 mg Eq AT/100g du PF.
d. Teneur en anthocyanes
Les anthocyanes sont des pigments phénoliques hydrophiles responsables de la coloration rouge, bleue ou violette de nombreux fruits et légumes. Les nutritionnistes recommandent la préservation de ces composés lors du procédé d’extraction du gel, vu leurs effets bénéfiques pour la santé (Orak, 2009; Shwartz et al., 2009).
Les résultats du dosage des anthocyanes sont présentés dans la figure suivante.
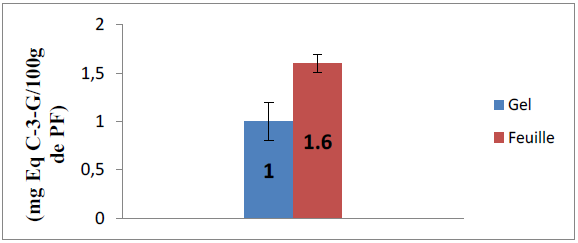
Figure 16 : Teneur en anthocyanes des extraits du gel et des feuilles d’Aloe arborescens
L’analyse statistique révèle que les résultats sont significativement déférents (P < 0,05).
Selon la figure ci-dessus, on constate que la concentration des anthocyanes dans les feuilles est égale à 1,16 ± 0,09 mg Eq C-3-G/100g du PF, supérieure à celle trouvée dans le gel égale à 1 ± 0,2 mg Eq C-3-G /100g du PF.
Nos résultats Sont légèrement supérieurs à ceux de Turner et ses collaborateurs (2004), l’extrait des feuilles d’Aloe arborescens contient 1,2 ± 0,2 mg Eq C-3-G / 100g du PF, alors que le gel contient 0,6 ± 0,03 mg Eq C-3-G /100g du PF.
Cette différence est probablement due aux condition de culture, au stade de maturité et à la méthode d’extraction (Ozgen et al., 2008).
e. Teneur en caroténoïdes
Les caroténoïdes sont insolubles dans l’eau et solubles dans les solvants organiques tels que l’acétone, le chloroforme (Rodriguez, 2005). Dans la présente étude, deux phases ont été utilisées : une phase apolaire qui permet de récupérer les caroténoïdes et une phase polaire pour éliminer les molécules hydrophiles tels que les polyphénols, particulièrement les flavonoïdes.
Les teneurs en caroténoïdes de nos extraits sont illustrées dans la figure 17.
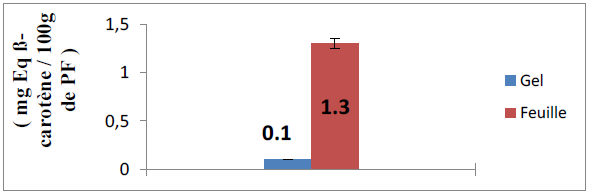
Figure 17 : Teneur en caroténoïdes des extraits du gel et des feuilles d’Aloe arborescens
Selon l’analyse statistique, les résultats sont significativement déférents (P < 0,05).
Selon la figure ci-dessus, les feuilles contiennent 1,3 ± 0,05 mg Eq β-carotène /100g du PF, cette concentration est supérieure à celle du gel qui contient 0,1 ± 0,003 mg Eq β-carotène /100g du PF.
Selon Bhattacharya et ses collaborateurs (2011), les concentrations en caroténoïdes du gel et de la feuille sont 1,12 ± 0,03 mg Eq β-carotène /100g du PF et 1,9 ± 0,01 mg Eq β-carotène /100g du PF respectivement. Ces concentrations sont supérieures à celles de nos échantillons ; ceci est probablement dû à la méthode d’extraction ou de dosage, la variété de la plante, la saison de récolte, le sol et aux conditions climatiques (Lee ,2012).
f. Analyse qualitative de l’aloïne par HPLC
Les chromatogramme obtenus concernant l’analyse qualitative de l’aloïne dans le gel et feuilles d’Aloe arborescens sont illustrés par la figure ci-dessous.
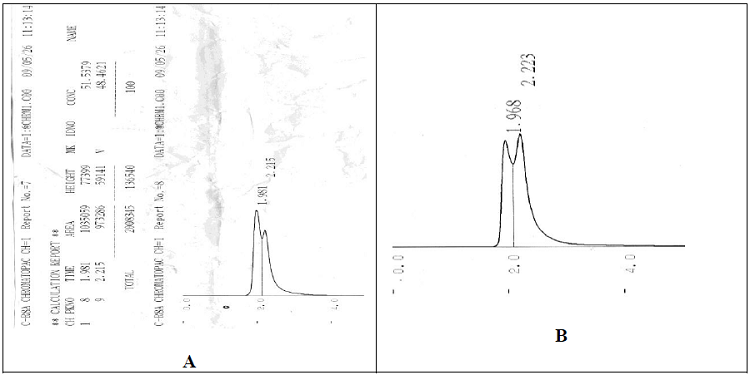
Figure 18 : Chromatogrammes de l’aloïne dans les feuilles (A) et dans le gel (B) d’Aloe arborescens
Ces chromatogrammes montrent la présence de deux piques pour chaque échantillon (gel et feuilles), car l’aloïne est composée de deux isomères : l’aloïne A et l’aloïne B.
Selon Himesh et ses collaborateurs (2011), qui ont comparé leurs résultats à un étalon (aloïne) ; le premier pique correspond à l’aloïne B (plus polaire) et le deuxième isomère à l’aloïne A.
D’après le chromatogramme A, l’aloïne B de la feuille a été élué après 1,981 min (1 min et 58 secondes) avec une hauteur de 77399 unités (concentration égale à 51,5379%) et le temps d’élution de l’aloïne A égale à 2,215 min (2 min et 12 secondes) avec une hauteur de 59141 unités (concentration égale à 48,4621%), la hauteur totale du pique (aloïne) est 136540 unités.
Selon le chromatogramme B, le temps d’élution de l’aloïne B est 1 min et 58,08 secondes avec une hauteur de 14621 (concentration égale à 48,5844%), alors que l’aloïne A a été élué après 2 min et 13 secondes avec une hauteur de 15473 unités (concentration égale à 51,4155%), la hauteur totale (aloïne) est 30094 unités.
Ses résultats sont différents de ceux de Himesh et ses collaborateurs (2011), en étudiant l’aloïne dans le gel d’Aloe vera par HPLC : l’aloïne B a été élué après 1min et 21 secondes avec un pourcentage de 96,3% et l’aloïne A après 2 min et 48 secondes avec un pourcentage de 3,7%.
On remarque aussi que la quantité d’aloïne trouvée dans la feuille est supérieure 4 fois comparée à celle du gel, avec un une différence de 106446 unités, cette différence est due selon Schweizer, (2006) à la répartition des cellules péricycliques (responsables de la formation de l’aloïne) qui se localisent dans la cuticule de la feuille et pas dans le gel.
Page suivante : II.6. Analyse microbiologique du gel et feuilles